Wie können Sie die Beschränkungen der endtidalen CO₂-Überwachung im Schlaflabor überwinden?
Wenn Schlaflaborteams die Beatmung überwachen möchten, müssen sie wissen, wie sich die Einschränkungen der endtidalen CO₂-Messung auf ihre Patienten auswirken können. In diesem Beitrag erläutern wir die Grundlagen der endtidalen CO₂-Messung, und wir untersuchen ihre klinischen Einsatzmöglichkeiten, sowie ihre Grenzen für die CO₂-Überwachung im Schlaflabor.
Wie können Sie die Beschränkungen der endtidalen CO₂-Überwachung im Schlaflabor überwinden?
Wenn Schlaflaborteams die Beatmung überwachen möchten, müssen sie wissen, wie sich die Einschränkungen der endtidalen CO₂-Messung auf ihre Patienten auswirken können. In diesem Beitrag erläutern wir die Grundlagen der endtidalen CO₂-Messung, und wir untersuchen ihre klinischen Einsatzmöglichkeiten, sowie ihre Grenzen für die CO₂-Überwachung im Schlaflabor.
Wie können Sie die Beschränkungen der endtidalen CO₂-Überwachung im Schlaflabor überwinden?
Wenn Schlaflaborteams die Beatmung überwachen möchten, müssen sie wissen, wie sich die Einschränkungen der endtidalen CO₂-Messung auf ihre Patienten auswirken können. In diesem Beitrag erläutern wir die Grundlagen der endtidalen CO₂-Messung, und wir untersuchen ihre klinischen Einsatzmöglichkeiten, sowie ihre Grenzen für die CO₂-Überwachung im Schlaflabor.
Was ist die endtidale CO₂-Überwachung und wie wird diese im Schlaflabor eingesetzt?
Die endtidale CO2-Überwachung im Schlaflabor ist eine nicht invasive und kontinuierliche Möglichkeit der Messung von CO2 am Ende eines jeden Atemzugs. Die primäre Funktion ist eine Messung von Atemzug zu Atemzug, um zum einen Apnoen zu identifizieren und zum anderen CO2 zu messen. Mit der kontinuierlichen Überwachung von Patienten im Schlaflabor erhalten KlinikerInnen einen besseren Überblick über den Beatmungsstatus ihrer Patienten.
Die Grenzen der endtidalen CO₂ Überwachung im Schlaflabor
Auch wenn die Kontinuität der endtidalen Überwachung einen Vorteil gegenüber der Blutgasmessung mittels Blutabnahmen darstellt, ist die Technologie mit Herausforderungen verbunden, wenn es darum geht, CO₂ genau zu messen. Dies gilt für das Schlaflabor insbesondere aus den folgenden Gründen:
- Die endtidale Messung unterschätzt häufig das CO₂ bei Patienten mit einem gestörten Ventilations-Perfusions-Verhältnis (V/Q-Verhältnis).
- Bei Patienten unter NIV kann der endtidale Wert den PaCO₂-Wert aufgrund von Gasmischung und Leckagen falsch darstellen.
- Bei Split-Night-Studien kann die endtidale Messung nur unzureichend kongruente Informationen liefern. Da sich die Beatmungsmethode ändern kann, ändert sich auch die Schätzung des PaCO₂ durch die endtidale Messung.
- Die Compliance der Patienten kann ein Problem darstellen, insbesondere bei pädiatrischen Patienten.
Hier werden wir etwas tiefer in einige dieser Herausforderungen eintauchen und wie sie überwunden werden können.
Endtidales CO₂ bei Patienten mit gestörtem V/Q-Verhältnis

Bei Patienten mit gesunder Lunge, die normal atmen, bietet etCO2 eine zuverlässige Schätzung des arteriellen CO2. Bei Patienten mit einem gestörten V/Q-Verhältnis ist etCO2 jedoch unzureichend. Dies liegt an der grundlegenden physiologischen Natur des gestörten Gasaustauschs, der durch ein gestörtes V/Q-Verhältnis verursacht wird.
Für eine ausführliche Diskussion zur CO2-Überwachung und zum V/Q-Missverhältnis, laden Sie unser Whitepaper herunter
Das CO2 in der Atemluft entspricht nicht dem CO2 im Blut
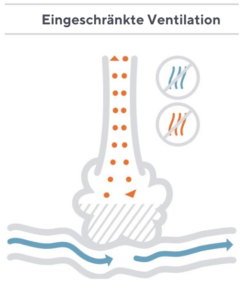
Betrachten wir einen hypothetischen Patienten mit Asthma, der aufgrund einer gestörten Ventilation eine gewisse Störung des V/Q-Verhältnisses aufweist. In diesem Fall strömt während der Einatmung zwar etwas Sauerstoff ein, aufgrund der eingeschränkten Luftzufuhr kann der Grossteil des Sauerstoffs die Alveolen jedoch nicht erreichen, und nur ein Teil diffundiert in den Blutkreislauf. Der Patient atmet das O2, das er gerade eingeatmet hat, grösstenteils wieder aus.
In der Zwischenzeit diffundiert das CO2 aus dem Blut des Patienten in die Lunge. Da aber der Luftstrom eingeschränkt ist, wird nur eine unbedeutende Menge ausgeatmet. Ein endtidaler Sensor misst dann eine verdünnte CO2-Probe in der ausgeatmeten Luft. Diese Messung ist nicht repräsentativ für den PaCO2-Wert. Der etCO2-Wert des Patienten ist niedriger als der PaCO2-Wert, der bei einer Blutentnahme gemessen wird – in einigen Fällen sogar deutlich niedriger.¹
Einfach ausgedrückt: Bei Patienten mit einer Störung des V/Q-Verhältnisses stimmt der CO2-Gehalt in der Atemluft nicht mit dem CO2-Gehalt im Blut überein, was die Genauigkeit der endtidalen Messung erheblich einschränkt. Eine Unterschätzung des CO2-Gehalts kann zu einem unzureichenden oder verzögerten Beatmungsmanagement des Patienten führen.

V/Q-Missverhältnis bei Patienten mit schlechter Perfusion
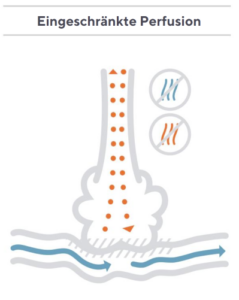
Bei Patienten mit schlechter Perfusion bringt die etCO2-Überwachung eine ähnliche Herausforderung mit sich. Bei einem hypothetischen Patienten, der mit Überdruck beatmet wird, können die Alveolen überdehnt werden, wodurch die Lungenkapillaren zusammengedrückt werden und die Perfusion eingeschränkt wird.
In diesem Szenario strömt die Luft durch die Atemwege zu den Alveolen, aber aufgrund der schlechten Perfusion besteht nur ein minimaler Blutfluss, in welchen der Sauerstoff diffundieren kann, und der Sauerstoff wird grösstenteils wieder ausgeatmet. Gleichzeitig diffundiert das CO2 nicht effektiv in die Lunge, sondern wird im Blutkreislauf zurückgehalten, wodurch sich der PaCO2-Wert des Patienten erhöht. Das Endergebnis ist das gleiche: Der CO2-Wert in der Atemluft stimmt nicht mit dem CO2-Wert im Blut überein, was bedeutet, dass der Endtidalwert den PaCO2-Wert unterschätzt. Auch in diesem Szenario kann eine Unterschätzung des CO2-Spiegels eines Patienten zu einem unzureichenden Management des Beatmungsstatus führen.
Präzise, kontinuierliche CO2-Überwachung für Patienten mit gestörtem V/Q-Verhältnis
Bei der transkutanen CO2-Überwachung wird ein nicht-invasiver Sensor verwendet, welcher die Haut an der Messstelle sanft auf 41 C° erwärmt. Dadurch wird die Durchblutung und die Diffusion von Gasen durch die Haut gefördert. Das CO2 gelangt durch eine durchlässige Membran auf der Sensoroberfläche in das speziell formulierte Elektrolyt, wo eine messbare Reaktion stattfindet. Proprietäre Algorithmen übersetzen die Daten dann in eine Schätzung des PaCO2.
Da bei der transkutanen Überwachung das CO2 über die Haut und nicht über die Atemluft gemessen wird, sind die alveoläre Perfusion und die Ventilation für die Genauigkeit der Messung irrelevant. Durch die Messung im Kapillarbett liefert tcPCO2 eine bessere Schätzung des PaCO2 und vermeidet weitgehend die Genauigkeitsprobleme bei einem gestörten V/Q-Verhältnis, die bei etCO2 auftreten.
Wie eine Forschergruppe in der Zeitschrift Critical Care Medicine feststellte, hat sich gezeigt, dass “die endtidale CO2-Überwachung bei Patienten mit normaler Lungenfunktion eine genaue Schätzung der Ventilation ermöglicht. Bei schwerkranken Patienten, bei denen die Lungenfunktion häufig gestört ist, ist diese Genauigkeit jedoch eingeschränkt, da intrapulmonale Shunts und ein erhöhter alveolärer Totraum zu einer ständigen Unterschätzung des PaCO2 führen. Umgekehrt ist die Genauigkeit der tcPCO2-Überwachung unabhängig vom Lungenstatus und kann einige der Probleme umgehen, die mit der etCO2-Überwachung verbunden sind.”²
Zu den Patienten, die häufig im Schlaflabor untersucht werden und bei denen eine Störung des V/Q-Verhältnisses in unterschiedlichem Ausmass auftreten kann, gehören Patienten mit Asthma, obstruktiver Schlafapnoe, COPD, chronischer Bronchitis, Lungenentzündung, pulmonaler Hypertonie, kollabierten Alveolen, Lungenembolie und mehr.
Wie wirkt sich die Gasmischung auf die endtidale CO₂-Überwachung im Schlaflabor aus?
Ähnlich wie die Störung des V/Q-Verhältnisses setzt das Problem der Gasmischung der endtidalen Überwachung Grenzen. Da bei der endtidalen Überwachung eine Atemprobe erfasst wird, ist es wichtig, daran zu denken, dass jede Änderung des Luftstroms über den endtidalen Sensor eine direkte Auswirkung auf die Messung hat – unabhängig davon, ob die Luft aus der Atemluft des Patienten oder aus einer anderen Quelle stammt oder nicht.
Bei Patienten, die an zusätzliche Beatmungsgeräte angeschlossen sind, ist der Luftstrom komplizierter, was zu einer weiteren Vermischung mit der ausgeatmeten Luft des Patienten führen kann. Anstelle einer reinen Probe der ausgeatmeten Luft des Patienten wird bei der endtidalen Messung dieses Gemisch erfasst.
Beispielsweise hat die endtidale Überwachung bei Patienten mit Kanüle oder BiPAP Schwierigkeiten, das arterielle CO₂ des Patienten genau wiederzugeben (selbst bei einem Patienten mit normalem V/Q-Verhältnis), da die Gasprobe in der Maske mehr als nur die ausgeatmete Luft des Patienten enthält. Was der Endtidale-CO₂-Sensor anzeigt, ist eine Mischung aus dem BiPAP-Flow und der Ausatemluft des Patienten. Dieser Wert ist für die Luft in der Lunge des Patienten oder für sein arterielles CO₂ nicht repräsentativ.
In Situationen, in denen eine Maske über einer Kanüle angebracht wird, kann es vorkommen, dass die Kanülenschläuche keine vollständige Abdichtung der Maske ermöglichen, wodurch Gas in die Maske bzw. aus der Maske entweicht, und die Luft, die der Endtidale-Sensor misst, weiter gestört wird.
Wie überwindet die transkutane Überwachung das Problem der Gasmischung?
Da die transkutane Überwachung nicht auf die Funktion der Atemwege oder eine Maskenschnittstelle angewiesen ist, kann sie die Probleme der Gasmischung und -verdünnung überwinden (sie vermeidet das Problem der Abhängigkeit von der Funktion der Atemwege und der Perfusion aufgrund eines gestörten V/Q-Verhältnisses) und einen CO₂-Wert überwachen, der den arteriellen CO₂-Wert des Patienten genau schätzt.
Ein transkutaner Sensor wird auf der Haut platziert und misst das CO₂ durch das Kapillarbett, wodurch eine genaue Schätzung des arteriellen CO₂ möglich ist.¹ʽ⁴ʽ⁵ Aus diesem Grund ist die transkutane CO₂-Überwachung völlig unabhängig von der Beatmungsmethode und wird nicht durch die Gasmischung in der Maske beeinträchtigt.
Wie kann endtidales CO₂ die Überwachung von Split-Night-Studien erschweren?
Wie Schlaftechnologen wissen, wird bei der Split-Night-Polysomnographie eine Maske (in der Regel CPAP) während eines Teils des Schlafzyklus des Patienten aufgesetzt. Dies geschieht, um den Unterschied des Atemzustands des Patienten zu bestimmen, wenn sie/er eine Beatmungsunterstützung erhält und wenn nicht.
Unter der Annahme, dass ein Patient keine Störung des V/Q-Verhältnisses aufweist, ist es für den Teil der Untersuchung ohne Maske möglich, einen genauen Messwert für das Endtidale-CO₂ zu erhalten, solange die Kanüle an Ort und Stelle bleibt und der Patient regelmässig atmet (was bei einem Patienten mit obstruktiver Schlafapnoe (OSA), die ihrerseits eine mögliche Ursache für ein V/Q-Missverhältnis ist, nicht der Fall sein kann).
Wenn die Hälfte einer Split-Night-Studie mit einer Maske durchgeführt wird, und die endtidale Messung aufgrund der oben genannten Probleme mit der Gasmischung Schwierigkeiten hat, die Genauigkeit aufrechtzuerhalten, dann wird der Teil der Schlafstudie unter Maske, wenn er mit der endtidalen Messung gemessen wird, wenig Aufschluss über den CO₂-Status des Patienten geben.
Im Verlauf einer Split-Night-Studie kann die Unzuverlässigkeit der endtidalen CO₂-Überwachung dazu führen, dass mehr Fragen als Antworten zum Beatmungsstatus Ihres Patienten entstehen:
- Wenn das CO₂ nach dem Aufsetzen der Maske gesunken ist, liegt das an der verbesserten Ventilation oder ist die endtidale Probe durch Gasmischung verdünnt?
- Wenn der Patient zu schnarchen beginnt und andere OSA-Symptome zeigt, ist dann die endtidale Messung aufgrund eines gestörten V/Q-Verhältnisses beeinträchtigt?
- Wenn sich der Patient während der Nacht bewegt oder besonders agitiert ist (z. B. ein Kleinkind), ist der Wert dann echt, oder wurde die Kanüle entfernt?
Wie bereits zu Beginn dieses Beitrags erwähnt, besteht einer der Hauptvorteile der endtidalen Messung darin, dass sie eine kontinuierliche CO₂-Überwachung ermöglicht. Dieser Vorteil geht verloren, wenn die Kontinuität der Daten in Frage gestellt wird, wie es bei der Überwachung von Split-Night-Studien, bei nicht-Compliance Ihrer Patienten oder bei Patienten mit V/Q-Missverhältnis der Fall ist.
Wie überwindet die transkutane Überwachung die Herausforderungen der Überwachung während der Nacht und bei Split-Night-Studien?
Wie oben beschrieben, hängt die Genauigkeit der transkutanen CO₂-Überwachung nicht von der gleichmässigen Beatmung des Patienten ab, da die Messung durch die Haut erfolgt. Die Genauigkeit der transkutanen CO₂-Messung hängt auch nicht davon ab, ob der Patient für einen Teil oder die gesamte Nacht eine Maske trägt oder nicht.
Da die transkutane Überwachung nicht von der Platzierung einer Kanüle abhängt, gibt es auch keine Probleme mit der Genauigkeit der transkutanen Überwachung bei Patienten, die das Tragen einer Kanüle als schwierig empfinden.
Das transkutane CO₂-Überwachungssystem von Sentec verfügt ausserdem über integrierte Funktionen, die Sie bei der zuverlässigen CO₂-Überwachung während der gesamten Nacht unterstützen, darunter:
- Smart Cal-Mem, mit dem der Sensor bis zu 30 Minuten lang vom Monitor getrennt und wieder angeschlossen werden kann, ohne dass eine Neukalibrierung erforderlich ist (d. h. Patienten können aufstehen, um auf die Toilette zu gehen, ohne dass eine (manchmal bis zu 14-minütige) Neukalibrierung zwischen CO₂-Sensor und Monitor erforderlich ist).
Erfahren Sie mehr über die klinischen Auswirkungen der CO₂-Messung im Schlaflabor
Die transkutane Technologie von Sentec überwindet die Grenzen der Pulsoximetrie, der arteriellen Blutentnahme und der Kapnographie mit einer kontinuierlichen CO₂-Überwachung. Sie kombiniert einfache Handhabung und Patientenkomfort mit genauen Werten unabhängig von der Beatmungsmethode oder eines Ventilations-Perfusions-Missverhältnisses, sowie mit Produktmerkmalen, die für die Schlafmedizin entwickelt wurden.
References:
- Cox, P., et al. Noninvasive Monitoring of PaCO2 during One-Lung Ventilation and Minimal Access Surgery in Adults: End-Tidal versus Transcutaneous Techniques. Journal of Minimal Access Surgery. 2007.
- Berkenbosch, J.W., Tobias, J. Transcutaneous Carbon Dioxide Monitoring During High-Frequency Oscillatory Ventilation in Infants and Children. Critical Care Medicine. 2002.
- Don, D., et al. Transcutaneous CO2 Monitoring in Children Undergoing Tonsillectomy for Sleep Disordered Breathing. The Laryngoscope. 2020.
- Schwarz, S.B., et al. Continuous Non-Invasive PCO2 Monitoring in Weaning Patients: Transcutaneous is Advantageous Over End-Tidal PCO2. Respirology. 2017.


